關於乳癌
乳癌是從乳腺的上皮細胞或小葉生長出來的一種惡性瘤,因癌細胞生長失去控制,若局部侵犯並破壞鄰近的組織及器官,則稱為「局部侵犯性乳癌」 ; 如果經由血液或淋巴系統轉移到其它器官,則稱為「轉移性乳癌」。
認識乳癌
- 為全球最常見的女性癌症,佔女性癌症的1/3,佔所有癌症的1/10
- 45~55歲女性最常見死因
- 台灣的發生率在過去20年內增加了約3倍(從每十萬人30人發生到90人發生)[1]
| 早期乳癌 | 晚期乳癌 | ||
| 第一期 | 第二期 | 第三期 | 第四期 |
| 五年存活率95% | 五年存活率85% | 五年存活率55% | 五年存活率15% |
| 乳房腫塊小於2公分,無腋下淋巴結轉移 | 乳房腫塊在2-5公分之間,可能有或沒有淋巴結轉移 | 乳房腫塊大於5公分,皮膚可能出現紅腫潰爛等變化,大部分腋下淋巴結轉移 | 不論腫瘤大小,有遠處器官轉移,如骨、肝、肺、腦等器官 |
| Ki-67 癌細胞複製能力 |
ER/PR(+)荷爾蒙受體陽性 | /PR(-) 荷爾蒙受體陰性 |
|
| 低(Ki-67<14%) | 高(Ki-67≥14%) | ||
| HER2受體陰性 | 管腔A型 | 管腔B型/HER2陰性 | 三陰性乳癌 佔所有乳癌患者13% |
| 佔所有乳癌病人73% | |||
| HER2受體陽性 | 管腔B型/HER2陽性 佔所有乳癌病人10% |
HER2陽性(非管腔型) 佔所有乳癌患者5% |
|
ER/PR(荷爾蒙受體):分為動情激素受體(ER)及黃體激素受體(PR)
乳癌細胞表面有荷爾蒙接受體的時候,會受到荷爾蒙的刺激而加速癌細胞成長。乳癌細胞含有越多的荷爾蒙接受體,對於荷爾蒙治療的效果越好,預後越佳。
HER2(人類表皮生長因子受體)
此受體過度表達會加速癌細胞分裂、增加轉移機率。因此,臨床醫師一定會檢測此受體(HER-2),作為治療及預後的參考。目前約有20%的病人在檢測此受體後,會呈現陽性反應,這類病人可使用標靶藥物進行治療。
Ki67(細胞增值指標)
常用來檢測細胞的增殖率,比例越高表示癌細胞的生長分裂速度越快。
- 乳房腫塊
- 乳房皮膚潰瘍或凹陷
- 乳房疼痛
- 乳房皮膚紅腫、結痂或變厚
- 乳頭疼痛或凹陷
- 乳頭有乳汁以外的分泌物
- 上臂異常腫脹
- 乳房附近淋巴結變大
參考資料:
治療方式
乳癌的治療需要腫瘤外科、病理科、腫瘤內科與放射腫瘤科專科醫師共同診斷與治療,乳癌期別是影響治療方式的主因,若癌細胞擴散,則需更多治療。但也有其他重要因素會影響治療選擇,如:
- 腫瘤細胞本身有無荷爾蒙接受體(hormone receptor)
- 腫瘤細胞本身的人類表皮生長因子第二型受體(HER2)含量
- 病人本身健康狀況與個人喜好
因此需與醫師詳細討論使用何種方式治療,治療方式對於病情的未來發展影響甚大。以早期乳癌來說,精準醫療時代的治療流程及治療方式如下:
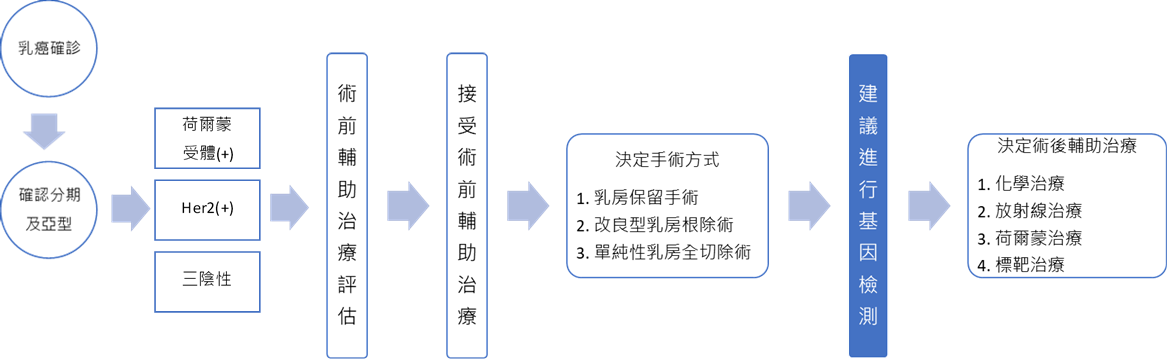
根據NCCN Guideline及台灣乳房醫學會BCST共識會議書面記錄建議:
- ER(+)Node(-)HER2(-)的病人如能以基因檢測證實低復發風險,則可考慮不做化療。
- 如1-3 Node(+)ER(+)HER2(-)的病人,能以基因檢測證實低復發風險,則可考慮不做化療。
- 可以考慮使用GnRH analogue治療停經前、高復發風險(包含小於40歲、Node(+)、T1c或以上且具備危險因子如G3或基因檢測高風險或IHC4定義為intermediate risk或以上),但未接受過化療的患者。
乳癌基因檢測已經成為早期乳癌復發風險評估標準之一。
早期乳癌通常都可以藉由手術切除,常見方法如下:
- 乳房保留術與前哨淋巴結切片:通常用於小於2公分,切除範圍較小的腫瘤,常需搭配術後放射治療,以減少未來局部復發風險。手術中會進行前哨淋巴結切片,若切片結果為陽性,則須再進行腋下淋巴結切除。
- 改良式乳房切除術併乳房重建術:切除整個乳房與腋下淋巴結,保留胸大肌以進行乳房重建手術。
手術治療常見副作用:
- 暫時性肌肉強度降低與活動受限
- 神經受損:手臂、肩膀、胸部之麻痺和刺痛
- 淋巴循環受阻:上肢腫脹
通常在手術切除後予以放射線治療,可降低未來局部復發風險。
放射線治療是利用高能量放射線破壞、阻止癌細胞生長。通常於術後進行5~6週,每週5天的治療。目前建議使用術後放射線治療的族群如下:
- 腫瘤侵犯超過4個淋巴結
- 腫瘤侵犯靠近淋巴結的周圍組織
- 腫瘤大於等於2公分
- 手術切除邊界不完全,可能還有殘餘癌組織
放射線治療常見副作用:
- 疲倦
- 皮膚紅、乾燥、敏感和發癢
- 增加未來發生心肌梗塞與二次肺癌機會
通常在手術切除後,還會予以化學治療,可降低未來殘餘癌症發生遠端轉移的機會。化學治療是利用毒殺細胞的藥物,造成癌症細胞死亡,也可能同時傷害到部分正常人體細胞,造成一些副作用。
治療通常會合併使用多種化學藥物,依據幾種不同亞型乳腺癌類別,有不同建議藥物組合:
- 荷爾蒙接受體(Hormone receptor:ER/PR)陽性或陰性
- 人類表皮第二型受體(HER2)陽性或陰性
- 荷爾蒙接受體與人類表皮第二型受體皆陰性
- 腫瘤大小
化學治療常見副作用:
- 短期副作用:噁心、嘔吐、掉頭髮、腹瀉、口腔炎、感染、出血或貧血等
- 長期副作用:二次癌症、心臟毒性、早期停經、不孕或意識改變等
用於荷爾蒙接受體陽性者,諾瓦得士錠(Tamoxifen)是目前最常被使用的藥物。
其副作用極少,偶爾臉潮紅、陰道分泌物或出血。但少數長時間使用,會造成未來靜脈血栓或子宮內膜癌風險增加,故建議不要使用超過5年。
即使有上述多種治療方式,但因先前的檢驗工具無法判斷哪些病人容易復發、需於術後進一步治療,常使醫師在擬定早期乳腺癌治療決策時面臨困境。而透過系統性文獻回顧(systemic review)可以瞭解,接受手術治療後,僅10~15%的病人再從化學治療與放射治療得到好處[1, 2],說明了其餘病人其實承受了不必要的治療及副作用。
幸運地,由於癌症基因分子生物學的進展,現在已有基因診斷工具,可協助醫師找到最適合每位病人的治療方式。針對不同病人,量身打造治療策略,即是所謂的個人化醫療/精準醫療。
參考資料:
乳癌與精準醫療
精準醫療(Precision Medicine)一詞最早於2011年11月由美國國家研究委員會(United States National Research Council, NRC)提出,也可稱為「個人化醫療」,是指除了透過傳統方法病人症狀描述及常規檢查,加上生物醫學檢測(如基因檢測、蛋白質檢測、代謝檢測等),並將個人資料(如性別、身高、體重、種族、過去病史、家族病史等)透過人體基因資料庫進行比對及分析,從中選出最適合病人的治療方法,達到治療效果最大化及副作用最小化。
- 個人化治療,效果更好
- 減少不必要的副作用
- 降低過度醫療的資源浪費
隨著基因分析技術的躍進,癌症治療也進入新紀元。過去,醫師只能從臨床病灶狀態,選擇對應的治療方式;現在已能透過基因檢測,分析出病人個人特有的基因突變特徵,協助醫師制訂正確的治療策略,不只提升了治療效果,還可改善病人的生活品質。
精準醫療應用於早期乳癌風險評估,可透過基因檢測工具,確定癌細胞的特性,準確預測早期乳癌病人,未來會發生「局部復發」及「遠端轉移」的風險,提供醫師與病人更全面精準的資訊,讓每一位病人能獲得最適合的個人化治療,減少整體醫療負擔、改善癌症治療成效、提升治療品質。
